কন্টেন্ট
রসায়নে, "আংশিক চাপ" বলতে বোঝায় যে গ্যাসের মিশ্রণে প্রতিটি গ্যাস তার চারপাশের বিরুদ্ধে যেমন একটি নমুনা বোতল, ডাইভিং বাতাসের একটি ট্যাঙ্ক বা বায়ুমণ্ডলের সীমাগুলির বিরুদ্ধে কার্যকর হয়। আপনি যদি মিশ্রণে প্রতিটি গ্যাসের চাপ গণনা করতে পারেন তবে আপনি যদি জানেন যে এটির কতটি পরিমাণ রয়েছে, এটি কোন পরিমাণে থাকে এবং এর তাপমাত্রা। তারপরে আপনি গ্যাসের মিশ্রণের মোট চাপ খুঁজে পেতে এই আংশিক চাপগুলি যুক্ত করতে পারেন, বা আপনি প্রথমে মোট চাপটি খুঁজে পেতে পারেন এবং তারপরে আংশিক চাপগুলি খুঁজে পেতে পারেন।
পদক্ষেপ
অংশ 1 এর 1: গ্যাসের বৈশিষ্ট্য বুঝতে
প্রতিটি গ্যাসকে "আদর্শ" গ্যাস হিসাবে বিবেচনা করুন। রসায়নের ক্ষেত্রে একটি আদর্শ গ্যাস হ'ল এটি অন্যান্য অণুগুলির প্রতি আকৃষ্ট না হয়ে অন্যান্য গ্যাসের সাথে যোগাযোগ করে। পৃথক অণু একে অপরকে আঘাত করতে পারে এবং কোনওভাবে বিকৃত না হয়ে বিলিয়ার্ড বলের মতো বাউন্স করতে পারে।
- ছোট ছোট জায়গাগুলিতে সংকুচিত হয়ে তারা বৃহত্তর অঞ্চলে প্রসারিত হওয়ার সাথে সাথে আদর্শ গ্যাসের চাপ বৃদ্ধি পায় increase এই সম্পর্কটিকে রবার্ট বয়েলের পরে বোয়লের আইন বলা হয়। এটি গাণিতিকভাবে কে = পি x ভি বা আরও সহজভাবে, কে = পিভি হিসাবে বর্ণনা করা হয়েছে, যেখানে কে স্থির সম্পর্কের প্রতিনিধিত্ব করে, পি চাপকে উপস্থাপন করে এবং ভি ভলিউমকে প্রতিনিধিত্ব করে।
- বিভিন্ন সম্ভাব্য ইউনিটের একটি ব্যবহার করে চাপগুলি নির্ধারণ করা যেতে পারে। একটি হ'ল পাস্কেল (পা), বর্গমিটারের উপরে প্রয়োগ করা নিউটন শক্তি হিসাবে সংজ্ঞায়িত। আরেকটি হ'ল বায়ুমণ্ডল (এটিএম), সমুদ্রপৃষ্ঠে পৃথিবীর বায়ুমণ্ডলের চাপ হিসাবে সংজ্ঞায়িত। 1 এটিমের একটি চাপ 101,325 পা সমান।
- ভলিউম বৃদ্ধি এবং হ্রাস হওয়ায় আদর্শ গ্যাসের তাপমাত্রা বৃদ্ধি পায়। এই সম্পর্কটিকে জ্যাক চার্লসের পরে চার্লসের আইন বলা হয় এবং গাণিতিকভাবে কে = ভি / টি হিসাবে বর্ণনা করা হয়, যেখানে কে স্থির পরিমাণ এবং তাপমাত্রার মধ্যে সম্পর্ককে প্রতিনিধিত্ব করে, ভি আবার ভলিউমকে প্রতিনিধিত্ব করে, এবং টি তাপমাত্রাকে প্রতিনিধিত্ব করে।
- এই সমীকরণের গ্যাসের তাপমাত্রা ডিগ্রি কেলভিনে দেওয়া হয়, যা গ্যাসের তাপমাত্রার ডিগ্রি সেলসিয়াসের সংখ্যায় 273 যোগ করে পাওয়া যায়।
- এই দুটি সম্পর্ককে একক সমীকরণে একত্রিত করা যায়: k = PV / T, যা পিভি = কেটি হিসাবেও লেখা যেতে পারে।

গ্যাসগুলি কী পরিমাণে পরিমাপ করা হয় তা নির্ধারণ করুন। গ্যাসের ভর ও আয়তন থাকে। ভলিউম সাধারণত লিটার (l) দিয়ে পরিমাপ করা হয় তবে দুটি ধরণের ভর থাকে।- প্রচলিত ভরগুলি গ্রামে পরিমাপ করা হয় বা, যদি যথেষ্ট পরিমাণে ভর থাকে তবে কেজি হয়।
- গ্যাসগুলির স্বল্পতার কারণে এগুলি আণবিক ভর বা মোলার ভর নামক ভর আকারেও পরিমাপ করা হয়। কার্বারের জন্য 12 এর মানের তুলনায় প্রতিটি পরমাণুর সাথে গ্যাস তৈরি করা যৌগের প্রতিটি পরমাণুর পারমাণবিক ওজনের যোগফল হিসাবে মোলার ভরকে সংজ্ঞায়িত করা হয়।
- যেহেতু পরমাণু এবং অণুগুলির সাথে কাজ করা খুব কম হয়, তাই গ্যাসের পরিমাণগুলি মোলগুলিতে সংজ্ঞায়িত করা হয়। প্রদত্ত গ্যাসে উপস্থিত মোলের সংখ্যা গলার ভর দ্বারা ভর ভাগ করে নির্ধারণ করা যেতে পারে এবং n অক্ষর দ্বারা প্রতিনিধিত্ব করা যেতে পারে।
- আমরা গ্যাসের সমীকরণে নির্বিচারে ধ্রুবক কে প্রতিস্থাপন করতে পারি এন এর পণ্য, মলের সংখ্যা (মোল) এবং একটি নতুন ধ্রুবক আর. সমীকরণটি এখন এনআর = পিভি / টি বা পিভি = এনআরটি লেখা যেতে পারে।
- আর মান গ্যাসগুলির চাপ, আয়তন এবং তাপমাত্রা পরিমাপ করতে ব্যবহৃত ইউনিটগুলির উপর নির্ভর করে। লিটারে ভলিউম, কেলভিনের তাপমাত্রা এবং বায়ুমণ্ডলের মধ্যে চাপ সনাক্ত করতে এর মান 0.0821 এল.এটিএম / কে.মোল। পরিমাপের ইউনিটগুলিতে বিভাজন বার এড়ানোর জন্য এটি এল 0.0821 এটিএম কে মলও লেখা যেতে পারে।

ডালটনের আংশিক চাপের আইনটি বুঝতে পারেন। রসায়নবিদ এবং পদার্থবিজ্ঞানী জন ডাল্টন দ্বারা বিকাশিত, যিনি প্রথমে রাসায়নিক উপাদানগুলির পরমাণু দ্বারা তৈরির ধারণাটি উন্নত করেছিলেন, ডাল্টনের আইন বলে যে একটি গ্যাস মিশ্রণের মোট চাপটি মিশ্রণের প্রতিটি গ্যাসের চাপের যোগফল।- ডাল্টনের আইন পি হিসাবে সমীকরণ হিসাবে লেখা যেতে পারে মোট = পি1 + পি2 + পি3... সমান চিহ্নের পরে যতগুলি সংযোজন রয়েছে সেখানে মিশ্রণে গ্যাস রয়েছে।
- ডালটনের আইন সমীকরণটি বাড়ানো যেতে পারে যখন গ্যাসগুলির সাথে কাজ করার সময় যার ব্যক্তিগত আংশিক চাপগুলি অজানা, তবে আমরা সেগুলির পরিমাণ এবং তাপমাত্রা জানি। গ্যাসের আংশিক চাপ একই চাপ হয় যদি একই পরিমাণ পাত্র কেবল পাত্রে গ্যাস ছিল।
- আংশিক চাপগুলির জন্য প্রতিটি, আমরা আদর্শ গ্যাস সমীকরণটি আবার লিখতে পারি যাতে সূত্রের পিভি = এনআরটি পরিবর্তে, আমরা সমান চিহ্নের বাম দিকে কেবল পি রাখতে পারি। এটি করার জন্য, আমরা উভয় পক্ষকে ভি দ্বারা ভাগ করব: পিভি / ভি = এনআরটি / ভি। বাম দিকে দুটি ভীস পি = এনআরটি / ভি রেখে একে অপরকে বাতিল করে দেয়
- তারপরে আমরা আংশিক চাপ সমীকরণের ডান পাশে প্রতিটি পি সাবস্ক্রাইব করে নিতে পারি: পিমোট = (এনআরটি / ভি) 1 + (এনআরটি / ভি) 2 + (এনআরটি / ভি) 3…
পার্ট 2 এর 2: আংশিক চাপ এবং তারপরে মোট চাপ গণনা করা

আপনি যে গ্যাসগুলি নিয়ে কাজ করছেন তার আংশিক চাপ সমীকরণটি সংজ্ঞায়িত করুন। এই গণনার উদ্দেশ্যে, আমরা একটি 2 লিটারের বেলুন ধরে যাতে তিনটি গ্যাস রয়েছে: নাইট্রোজেন (এন2), অক্সিজেন (ও2) এবং কার্বন ডাই অক্সাইড (সিও)2)। প্রতিটি গ্যাসের মধ্যে 10 গ্রাম থাকে এবং ফ্লাস্কে প্রতিটির তাপমাত্রা 37º সেলসিয়াস হয়। আমাদের প্রতিটি গ্যাসের আংশিক চাপ এবং মিশ্রণটি ধারকটিতে প্রয়োগ করা মোট চাপ খুঁজে পাওয়া দরকার।- আমাদের আংশিক চাপ সমীকরণ পি হয় মোট = পি নাইট্রোজেন + পি অক্সিজেন + পি কার্বন - ডাই - অক্সাইড .
- যেহেতু আমরা প্রতিটি গ্যাস যে চাপ প্রয়োগ করে তা আবিষ্কার করার চেষ্টা করছি, আমরা ভলিউম এবং তাপমাত্রা জানি এবং আমরা খুঁজে পাই যে প্রতিটি গ্যাসের কতগুলি মলের ভর ভিত্তিতে উপস্থিত থাকে, তাই আমরা এই সমীকরণটি আবার লিখতে পারি: পিমোট = (এনআরটি / ভি) নাইট্রোজেন + (এনআরটি / ভি) অক্সিজেন + (এনআরটি / ভি) কার্বন - ডাই - অক্সাইড

তাপমাত্রা কেলভিনে রূপান্তর করুন। তাপমাত্রা 37º সেলসিয়াস, সুতরাং 310 কে পেতে 273 থেকে 37 যোগ করুন।
নমুনায় প্রতিটি গ্যাসের জন্য মলের সংখ্যা সন্ধান করুন। কোনও গ্যাসের মোলের সংখ্যা হ'ল গ্যাসের ভরকে তার মোলার ভর দিয়ে বিভক্ত করা হয়, যা আমরা বলেছিলাম যৌগের প্রতিটি পরমাণুর পারমাণবিক ওজনের যোগফল।
- প্রথম গ্যাসের জন্য নাইট্রোজেন (এন।)2), প্রতিটি পরমাণুর পারমাণবিক ওজন ১৪. যেহেতু নাইট্রোজেন ডায়াটমিক (দুটি পরমাণুর আণবিক রূপ), তাই আমাদের নমুনায় নাইট্রোজেনের একটি দারু ভর ২৮ রয়েছে তা খুঁজে পেতে আমাদেরকে ১৪ দ্বারা ২ গুণ করতে হবে। তারপরে, ভরকে ভাগ করুন গ্রামে, 10 গ্রাম, 28-এর মধ্যে, মলের সংখ্যা পাওয়ার জন্য, যা আমরা প্রায় নাইট্রোজেনের 0.4 মোল will
- দ্বিতীয় গ্যাসের জন্য অক্সিজেন (ও2), প্রতিটি অণুটির পারমাণবিক ওজন 16 টি O অক্সিজেনটি ডায়াটমিকও হয়, সুতরাং আমাদের নমুনায় অক্সিজেনের 32 টির একটি গুড় ভর রয়েছে তা আবিষ্কার করতে 16 কে 2 দিয়ে গুণা করুন 32 32 দ্বারা 10 গ্রাম ভাগ করা আমাদের প্রায় অক্সিজেনের 0.3 মল দেয় নমুনা।
- তৃতীয় গ্যাস, কার্বন ডাই অক্সাইড (সিও)2), এর 3 পরমাণু রয়েছে: একটি কার্বন, 12 এর পারমাণবিক ওজন সহ; এবং দুটি অক্সিজেন, প্রতিটির 16 টি পারমাণবিক ওজন সহ। আমরা তিনটি ওজন যুক্ত করি: 12 + 16 + 16 = 44 মোরার ভরগুলির জন্য। 10 গ্রাম 44 দ্বারা ভাগ করা আমাদের প্রায় 0.2 মোল কার্বন ডাই অক্সাইড দেয়।

মোলস, ভলিউম এবং তাপমাত্রা দিয়ে মানগুলি প্রতিস্থাপন করুন। আমাদের সমীকরণটি এখন এটির মতো দেখাচ্ছে: পিমোট = (0.4 * আর * 310/2) নাইট্রোজেন + (0.3 0.3 * আর * 310/2) অক্সিজেন + (0.2 * আর * 310/2) কার্বন - ডাই - অক্সাইড.- সরলতার জন্য, আমরা মানগুলির সাথে পরিমাপের এককগুলি রেখেছি। আমরা গণিত করার পরে এই ইউনিটগুলি বাতিল করা হবে, চাপগুলি প্রতিবেদন করার জন্য আমরা যে পরিমাপ করছি তার কেবল এককটি রেখে চলেছি।
ধ্রুবক আর এর জন্য মানটি প্রতিস্থাপন করুন। আমরা বায়ুমণ্ডলে আংশিক এবং মোট চাপ খুঁজে পাব, সুতরাং আমরা 0.0821 এটি এল / কে.মোল এর আর মানটি ব্যবহার করব। সমীকরণে মান প্রতিস্থাপন এখন আমাদের পি দেয় givesমোট =(0,4 * 0,0821 * 310/2) নাইট্রোজেন + (0,3 *0,0821 * 310/2) অক্সিজেন + (0,2 * 0,0821 * 310/2) কার্বন - ডাই - অক্সাইড .
প্রতিটি গ্যাসের জন্য আংশিক চাপ গণনা করুন। এখন যেহেতু আমাদের জায়গাগুলির মান আছে, এখন এটি গণিত করার সময়।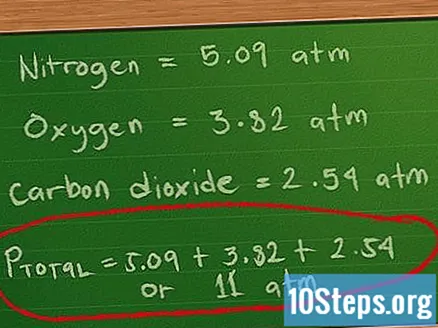
- নাইট্রোজেনের আংশিক চাপের জন্য, আমরা আমাদের 0.0821 ধ্রুবক এবং আমাদের 310 কে তাপমাত্রার দ্বারা 0.4 মলকে গুণিত করি এবং তারপরে 2 লিটার দিয়ে বিভক্ত করি: 0.4 * 0.0821 * 310/2 = 5, 09 এটিএম, আনুমানিক।
- আংশিক অক্সিজেন চাপের জন্য, আমরা আমাদের ০.০৮২২ ধ্রুবক এবং আমাদের 310 কে তাপমাত্রার দ্বারা 0.3 মলকে গুণিত করি এবং তারপরে 2 লিটার দ্বারা ভাগ করে: 0.3 0.3 * 0.0821 * 310/2 = 3, 82 এটিএম, প্রায়।
- কার্বন ডাই অক্সাইডের আংশিক চাপের জন্য, আমরা আমাদের 0.0821 ধ্রুবক এবং আমাদের 310 কে তাপমাত্রার দ্বারা 0.2 মলকে গুণিত করি এবং তারপরে 2 লিটার দ্বারা ভাগ করে: 0.2 * 0.0821 * 310/2 = 2.54 এটিএম, প্রায়।
- মোট চাপ খুঁজে পেতে এখন আমরা এই চাপগুলি যুক্ত করি: পিমোট = 5.09 + 3.82 + 2.54, বা প্রায় 11.45 এটিএম।
পার্ট 3 এর 3: মোট চাপ এবং তারপরে আংশিক চাপ গণনা করা হচ্ছে
পূর্বের মতো আংশিক চাপ সমীকরণটি সংজ্ঞায়িত করুন। আবার, আমরা ধরে নিই যে 2 লিটারের ফ্লাস্কে 3 টি গ্যাস রয়েছে: নাইট্রোজেন (এন)2), অক্সিজেন (ও2), এবং কার্বন ডাই অক্সাইড (CO2)। প্রতিটি গ্যাসের মধ্যে 10 গ্রাম থাকে এবং ফ্লাস্কের প্রতিটি গ্যাসের তাপমাত্রা 37 ডিগ্রি সেলসিয়াস হয়।
- কেলভিনের তাপমাত্রা এখনও 310 থাকবে এবং আগের মতোই আমাদের কাছে প্রায় 0.4 মোল নাইট্রোজেন, 0.3 মিলি অক্সিজেন এবং 0.2 মিলি কার্বন ডাই অক্সাইড রয়েছে।
- তেমনি, আমরা এখনও বায়ুমণ্ডলে চাপ খুঁজে পাব, তাই আমরা ধ্রুবক আর এর জন্য 0.0821 এটিএম এল / কে.মোলের মানটি ব্যবহার করব
- সুতরাং, আমাদের আংশিক চাপ সমীকরণটি এখনও এই সময়ে একই দেখাচ্ছে: পিমোট =(0,4 * 0,0821 * 310/2) নাইট্রোজেন + (0,3 *0,0821 * 310/2) অক্সিজেন + (0,2 * 0,0821 * 310/2) কার্বন - ডাই - অক্সাইড.
নমুনায় প্রতিটি গ্যাসের তিলের সংখ্যা যোগ করুন গ্যাসের মিশ্রণের মোট মোলগুলি খুঁজে বের করতে। যেহেতু গ্যাসের প্রতিটি নমুনার জন্য ভলিউম এবং তাপমাত্রা সমান, তাই প্রতিটি দারার মান একই ধ্রুবক দ্বারা গুণিত হয় তা উল্লেখ না করে আমরা পি হিসাবে সমীকরণটি পুনরায় লিখতে গণিতের বিতরণকারী সম্পত্তিটি ব্যবহার করতে পারিমোট = (0,4 + 0,3 + 0,2) * 0,0821 * 310/2.
- গ্যাস মিশ্রণের 0.4 + 0.3 + 0.2 = 0.9 মোল যোগ করা। এটি পি এর সমীকরণটিকে আরও সরল করে মোট = 0,9 * 0,0821 * 310/2.
গ্যাস মিশ্রণের মোট চাপ গণনা করুন। ০.৯ * 0.0821 * 310/2 = 11.45 মল প্রায় গুণমান।
মোট মিশ্রণে প্রতিটি গ্যাসের অনুপাত খুঁজুন। এটি করার জন্য, প্রতিটি গ্যাসের জন্য মলের সংখ্যাটি মোট মোলের সাথে ভাগ করুন।
- এখানে নাইট্রোজেনের 0.4 মোল রয়েছে, সুতরাং প্রায় 0.4 / 0.9 = 0.44 (44%) নমুনা।
- নাইট্রোজেনের ০.০ মোল রয়েছে, সুতরাং প্রায় নমুনার ০.০ / ০.৯ = ০.৩৩ (৩৩%)।
- কার্বন ডাই অক্সাইডের 0.2 মোল থাকে, সুতরাং প্রায় 0.2 / 0.9 = 0.22 (22%) নমুনা।
- যদিও উপরের আনুমানিক শতাংশগুলি কেবল 0.99 পর্যন্ত যোগ করে, প্রকৃত দশমিকগুলি পুনরাবৃত্তি হয়, সুতরাং প্রকৃত যোগফল দশমিকের পরে নাইনগুলির পুনরাবৃত্তির একটি সিরিজ। সংজ্ঞা অনুসারে, এটি 1, বা 100% এর সমান।
আংশিক চাপ সন্ধানের জন্য মোট চাপ দ্বারা প্রতিটি গ্যাসের আনুপাতিক মানকে গুণ করুন।
- 0.44 * 11.45 = 5.04 এটিএম প্রায় গুণমান।
- প্রায় 0.33 * 11.45 = 3.78 এটিকে গুণমান।
- প্রায় 0.22 11 * 11.45 = 2.52 এটিএম গুণমান।
পরামর্শ
- প্রথমে আংশিক চাপগুলি খুঁজে বের করে, তারপরে মোট চাপটি এবং প্রথমে মোট চাপ এবং তারপরে আংশিক চাপগুলি খুঁজে বের করে আপনি মানগুলির মধ্যে একটি ছোট পার্থক্য লক্ষ্য করবেন। মনে রাখবেন যে মানগুলি বুঝতে আরও সহজ করার জন্য এক বা দুটি দশমিক স্থানে গোল করার কারণে প্রদত্ত মানগুলি আনুমানিক মান হিসাবে উপস্থাপিত হয়েছিল। আপনি যদি কোনও ক্যালকুলেটর দিয়ে গণনাগুলি করেন, গোল না করে, আপনি দুটি পদ্ধতির মধ্যে তাত্পর্য দেখবেন a
সতর্কতা
- আংশিক গ্যাসের চাপ জ্ঞান ডাইভারের জন্য জীবন ও মৃত্যুর বিষয় হয়ে উঠতে পারে। অক্সিজেনের খুব কম আংশিক চাপ চেতনা এবং মৃত্যুর কারণ হতে পারে, যখন হাইড্রোজেন বা অক্সিজেনের একটি খুব উচ্চ আংশিক চাপও বিষাক্ত হতে পারে।
প্রয়োজনীয় উপকরণ
- ক্যালকুলেটর;
- পারমাণবিক ওজন / গুড় জনতার রেফারেন্স বই।