কন্টেন্ট
- পর্যায়ে
- পদ্ধতি 1 ট্রায়াল এবং ত্রুটি পদ্ধতি দ্বারা একটি সমীকরণ ভারসাম্যপূর্ণ
- পদ্ধতি 2 বীজগণিত পদ্ধতিতে একটি সমীকরণকে সামঞ্জস্য করুন
রসায়নে কোনও সমীকরণ রাসায়নিক বিক্রিয়াকরণের সময় ঘটেছিল তা প্রতিষ্ঠিত করে। সমীকরণের বাম দিকে, আমরা পরীক্ষাগুলির জন্য এবং ডানদিকে, পরীক্ষার সময় প্রাপ্ত পণ্যগুলি ব্যবহার করেছিলাম এমন রিজেন্টগুলি রাখি। রাসায়নিক বিক্রিয়া চলাকালীন ভর সংরক্ষণের নীতি অনুসারে (লাভায়েসিয়র) কোনও পরমাণু অদৃশ্য হয় না, কোনওটিই তৈরি হয় না, তারা আলাদাভাবে একত্রিত হয়। সংক্ষেপে, আপনার সমীকরণের বাম দিকে ডানদিকে প্রতিটি উপাদানের একই সংখ্যার ডেটোম থাকতে হবে। এজন্য একটি ভারসাম্য সমীকরণ সর্বদা ভারসাম্যপূর্ণ হতে হবে।
পর্যায়ে
পদ্ধতি 1 ট্রায়াল এবং ত্রুটি পদ্ধতি দ্বারা একটি সমীকরণ ভারসাম্যপূর্ণ
-
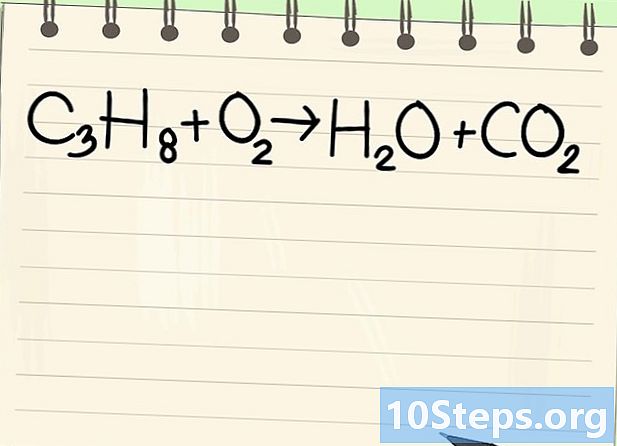
ভারসাম্য সমীকরণ নোট করুন। আমরা নিম্নলিখিত সমীকরণটি আচরণ করব:- সি3এইচ8 + ও2 -> এইচ2O + CO2
- এটি প্রোপেন দাহনের সমীকরণ (সি3এইচ8) অক্সিজেন: জল এবং কার্বন ডাই অক্সাইড প্রাপ্ত হয়।
-
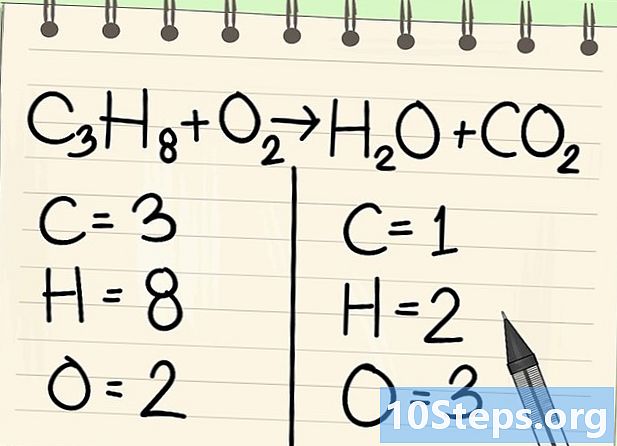
পরমাণু গণনা করুন। সমীকরণের একদিকে প্রতিটি এলিমেন্টের ডেটোমের সংখ্যা লিখুন, তারপরে অন্যটি। এর জন্য সূচকগুলি বিবেচনা করুন, যদি কিছু না থাকে তবে সূচকটি 1 হয়।- বাম দিকে, 3 টি কার্বন পরমাণু, 8 হাইড্রোজেন এবং 2 অক্সিজেন রয়েছে।
- ডানদিকে, কার্বনের 1 টি পরমাণু, হাইড্রোজেনের 2 এবং অক্সিজেনের 3 টি রয়েছে।
-
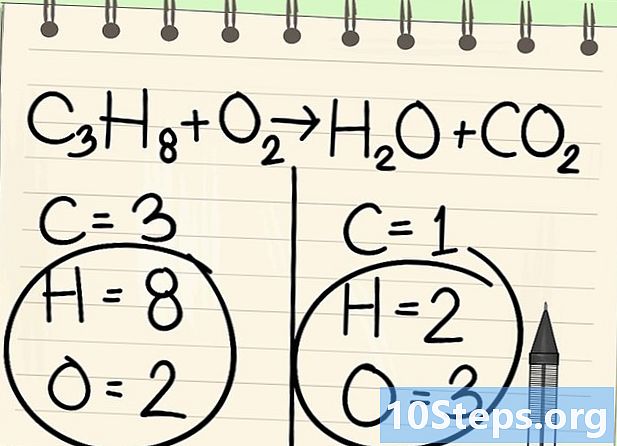
ক্ষণিকের জন্য হাইড্রোজেন এবং অক্সিজেনকে ছেড়ে দিন। -

সঠিক উপাদান দিয়ে ভারসাম্য শুরু করুন। আমরা সবসময় প্রতিক্রিয়ার আগে এবং পরে অণুতে একটি দিয়ে শুরু করি। যদি বেশ কয়েকটি থাকে তবে যে কোনও একটি অণুতে মনোভ্যালেন্ট এমন একটি নিন। এখানে আমরা কার্বন পরমাণু দিয়ে শুরু করি। -

কার্বন পরমাণুর ভারসাম্য রক্ষা করুন। ডানদিকে কার্বন ডাই অক্সাইড অণু (সিও) এর একটি সহগ যোগ করুন2) যার মধ্যে কার্বন ল্যাটোম একা। 3 টি বাম পরমাণু পেতে আমরা একটি 3 রেখে দেব।- সি3এইচ8 + ও2 -> এইচ2ও + 3সিও2
- সহগের (3CO) ডান ধন্যবাদ হিসাবে আমাদের কাছে 3 টি কার্বন পরমাণু রয়েছে2) এবং বাম দিকে 3 কার্বন পরমাণু সূচককে ধন্যবাদ জানায় (সি3এইচ8).
- একটি সমীকরণে, আপনি চান সমস্ত সহগগুলি রাখতে পারেন, তবে আপনি সূত্রগুলি স্পর্শ করতে পারবেন না।
-
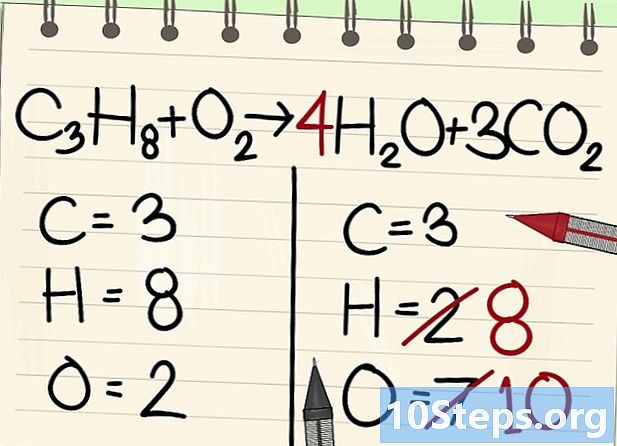
হাইড্রোজেন পরমাণুর ভারসাম্য রক্ষা করুন। আপনার যেমন সমীকরণের 8 টি বাম রয়েছে, আপনার ততটুকু ডান প্রয়োজন।- সি3এইচ8 + ও2 --> 4এইচ2O + 3CO2
- ডানদিকে, আপনি 4 এর সহগ রাখবেন, কারণ হাইড্রোজেন পানির অণুতে দ্বিখণ্ডিত: সূচক 2 নির্দেশ করে যে দুটি হাইড্রোজেন পরমাণু জড়িত।
- ডানদিকে হাইড্রোজেন পরমাণুর সংখ্যা পেতে, আপনি সহগের 4 টি সূচক 2 বা 8 পরমাণুর দ্বারা গুণিত করুন।
- অক্সিজেনের পরমাণু হিসাবে, ডানদিকে, 3CO এর তিনটি অণু থেকে একদিকে এখন 6 টি রয়েছে2 (3 এক্স 2 = 6 পরমাণু) এবং 4 এইচ এর 4 অণু থেকে 42ও (4 x 1 = 4 পরমাণু), অর্থাৎ অক্সিজেনের মোট 10 পরমাণু।
-
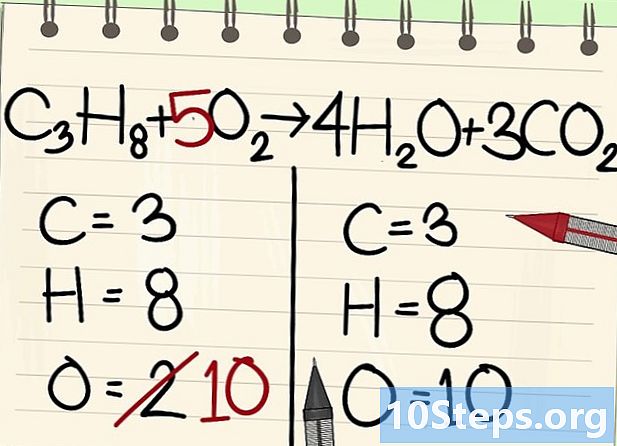
অক্সিজেনের পরমাণুর ভারসাম্য রক্ষা করুন।- কার্বন এবং হাইড্রোজেন ভারসাম্যের কারণে সমীকরণের উভয় পক্ষেই অক্সিজেন পরমাণুর সংখ্যা এক নয়। আমরা আগে দেখেছি যে ডানদিকে অক্সিজেনের 10 টি পরমাণু ছিল (জলের অণু থেকে 4, এবং কার্বন ডাই অক্সাইড অণু থেকে 6)। বাম দিকে, কেবল 2 (ও থেকে)2).
- অক্সিজেনের ভারসাম্য বজায় রাখতে, বাম অক্সিজেনের অণুতে 5 এর সহগ যুক্ত করুন: আপনার বাম দিকে অক্সিজেনের 10 টি পরমাণু রয়েছে এবং অন্যটি ডানদিকে রয়েছে।
- সি3এইচ8 + 5হে2 -> 4 এইচ2O + 3CO2
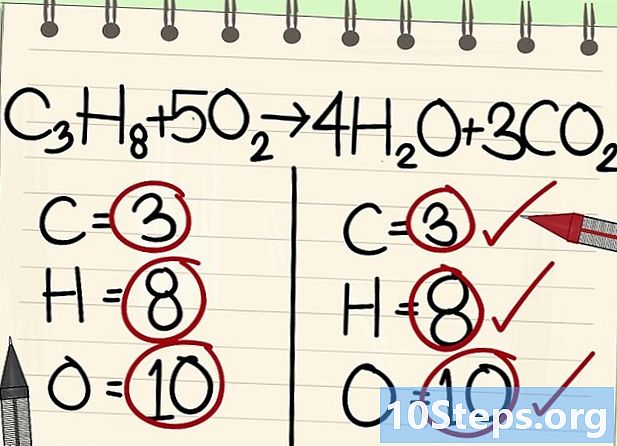
- সমস্ত পরমাণু (কার্বন, হাইড্রোজেন এবং অক্সিজেন) সুষম: আপনার সমীকরণ ভারসাম্যপূর্ণ।
পদ্ধতি 2 বীজগণিত পদ্ধতিতে একটি সমীকরণকে সামঞ্জস্য করুন
-

ভারসাম্য সমীকরণ লিখুন। প্রতিটি অণুতে একটি আক্ষরিক সহগ নির্ধারণ করুন। আমরা তাদের কল করব হয়েছে, খ, গ এবং ঘ. -
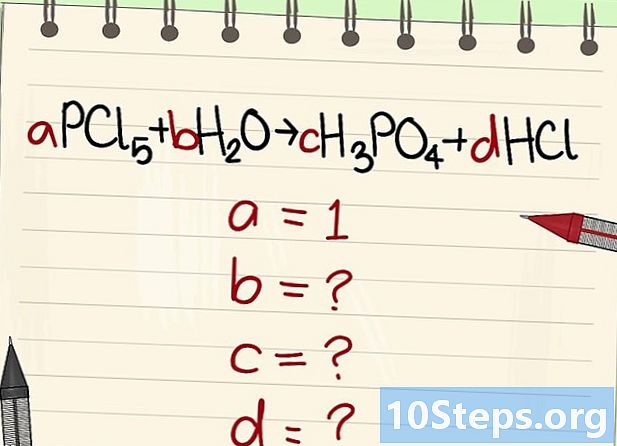
অন্যান্য আক্ষরিক সহগের মানটি সন্ধান করুন। আমরা এটা জিজ্ঞাসা করব হয়েছে = 1. -

এই সহগের মধ্যে সম্পর্কগুলি সন্ধান করুন। বাম (রিএজেন্টস) এবং ডান (পণ্য) খুঁজছেন, এই বিভিন্ন সহগের মধ্যে সম্পর্ক স্থাপন করুন।- নিম্নলিখিত সমীকরণটি গ্রহণ করুন: aPCl5 + bH2O = cH3PO4 + dHCl। এটি বলা হয়েছে যে a = 1, যার অর্থ সি = এ, ডি = 5 এ এবং 2 বি = 3 সি + ডি। গণনা করা হয়েছে, সি = 1, ডি = 5 এবং বি = 4।

- নিম্নলিখিত সমীকরণটি গ্রহণ করুন: aPCl5 + bH2O = cH3PO4 + dHCl। এটি বলা হয়েছে যে a = 1, যার অর্থ সি = এ, ডি = 5 এ এবং 2 বি = 3 সি + ডি। গণনা করা হয়েছে, সি = 1, ডি = 5 এবং বি = 4।