কন্টেন্ট
অন্যান্য বিভাগরসায়নে, যথোপযুক্ত সৃষ্টিকর্তা এমন একটি বৈদ্যুতিন যা কোনও উপাদানের বহিরাতমতম ইলেক্ট্রন শেলের মধ্যে অবস্থিত। কোনও নির্দিষ্ট পরমাণুতে ভ্যালেন্স ইলেকট্রনের সংখ্যা কীভাবে সন্ধান করা যায় তা জেনে রাখা রসায়নবিদদের কাছে একটি গুরুত্বপূর্ণ দক্ষতা কারণ এই তথ্যটি যে ধরনের রাসায়নিক বন্ধনগুলি গঠন করতে পারে তা নির্ধারণ করে এবং তাই উপাদানটির প্রতিক্রিয়া। ভাগ্যক্রমে, আপনাকে কোনও এলিমেন্টের ভ্যালেন্স ইলেক্ট্রনগুলি সন্ধান করতে হবে তা হ'ল উপাদানগুলির একটি আদর্শ পর্যায় সারণী।
পদক্ষেপ
2 এর 1 ম অংশ: একটি পর্যায় সারণী সহ ভ্যালেন্স ইলেকট্রন সন্ধান করা
অ-স্থানান্তর ধাতু
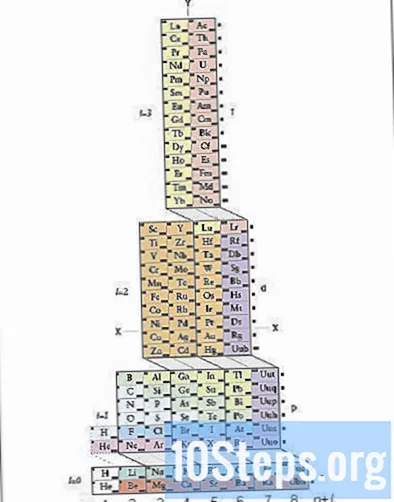
একটি উপাদানগুলির পর্যায় সারণি. এটি একটি বর্ণ-কোডেড টেবিল যা বিভিন্ন স্কোয়ার দ্বারা গঠিত যা মানবজাতির জন্য পরিচিত সমস্ত রাসায়নিক উপাদানগুলির তালিকা করে। পর্যায় সারণী উপাদানগুলির সম্পর্কে প্রচুর তথ্য প্রকাশ করে - আমরা যে তদন্ত করছি তার মধ্যে ভ্যালেন্স ইলেক্ট্রনের সংখ্যা নির্ধারণ করতে আমরা এই তথ্যগুলির কয়েকটি ব্যবহার করব। আপনি সাধারণত এগুলি রসায়ন পাঠ্যপুস্তকের প্রচ্ছদে খুঁজে পেতে পারেন। অনলাইনে এখানে একটি দুর্দান্ত ইন্টারেক্টিভ টেবিল উপলব্ধ।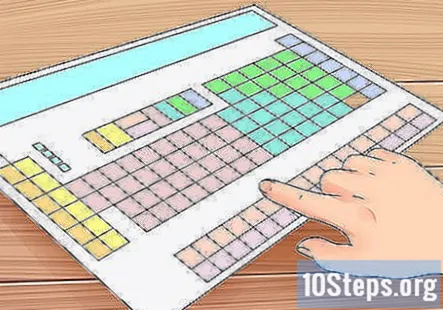

1 থেকে 18 পর্যন্ত উপাদানগুলির পর্যায় সারণীতে প্রতিটি কলাম লেবেল করুন। সাধারণত, পর্যায় সারণীতে, একটি একক উল্লম্ব কলামে সমস্ত উপাদানগুলির মধ্যে একই সংখ্যক ভ্যালেন্স ইলেকট্রন থাকে। যদি আপনার পর্যায় সারণীতে ইতিমধ্যে প্রতিটি কলামের সংখ্যা নেই, তবে প্রতিটি বাম প্রান্তটি 1 দিয়ে এবং প্রথম ডান প্রান্তে 18 দিয়ে শুরু করে প্রতিটি নম্বর দিন। বৈজ্ঞানিক ভাষায়, এই কলামগুলিকে উপাদান বলা হয় "গোষ্ঠী।"- উদাহরণস্বরূপ, যদি আমরা একটি পর্যায় সারণি নিয়ে কাজ করতাম যেখানে গ্রুপগুলি সংখ্যাযুক্ত নয়, আমরা হাইড্রোজেন (এইচ) এর উপরে একটি 1 লিখব, বেরিলিয়াম (বি) এর উপরে 2, এবং হেলিয়ামের উপরে 18 (18) না লিখে তিনি লিখবেন (তিনি) ।
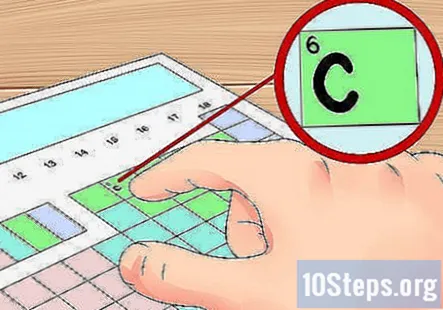
টেবিলে আপনার উপাদানটি সন্ধান করুন। এখন, আপনি যে উপাদানটি টেবিলের জন্য ভ্যালেন্স ইলেকট্রনগুলি সন্ধান করতে চান তা সন্ধান করুন। আপনি এটির রাসায়নিক প্রতীক (প্রতিটি বাক্সের অক্ষর), এর পারমাণবিক সংখ্যা (প্রতিটি বাক্সের উপরের বামে সংখ্যা), বা টেবিলে আপনাকে উপলভ্য তথ্যের যে কোনও টুকরো দিয়ে এটি করতে পারেন।- উদাহরণস্বরূপ, আসুন খুব সাধারণ উপাদানটির জন্য ভ্যালেন্স ইলেকট্রনগুলি সন্ধান করা যাক: কার্বন (সি) এই উপাদানটির একটি পারমাণবিক সংখ্যা 6 রয়েছে এটি 14 টি গ্রুপের শীর্ষে অবস্থিত the
- এই উপচ্ছেদে, আমরা ট্রানজিশনাল ধাতুগুলি উপেক্ষা করব, যা 3 থেকে 12 টি গ্রুপ দ্বারা নির্মিত আয়তক্ষেত্রাকার আকৃতির ব্লকের উপাদানগুলি এই উপাদানগুলি বাকী থেকে কিছুটা আলাদা, সুতরাং এই বিভাগের পদক্ষেপগুলি জিতেছে ' তাদের উপর কাজ। নীচের অনুচ্ছেদে এগুলি কীভাবে মোকাবেলা করবেন তা দেখুন।
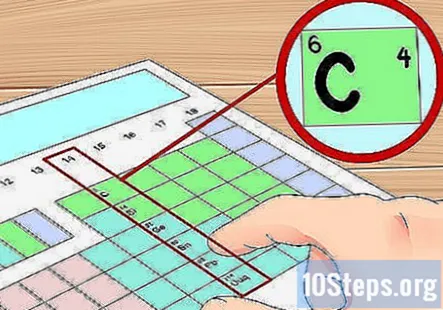
ভ্যালেন্স ইলেকট্রনের সংখ্যা নির্ধারণের জন্য গ্রুপ নম্বরগুলি ব্যবহার করুন। একটি অ-স্থানান্তর ধাতুর গ্রুপ নম্বরটি সেই উপাদানটির একটি পরমাণুতে ভ্যালেন্স ইলেকট্রনের সংখ্যা খুঁজে পেতে ব্যবহার করা যেতে পারে। দ্য গ্রুপ নম্বর লোকদের স্থান এই উপাদানগুলির একটি পরমাণুতে ভ্যালেন্স ইলেকট্রনের সংখ্যা। অন্য কথায়:- গ্রুপ 1: 1 ভ্যালেন্স ইলেক্ট্রন
- গ্রুপ 2: 2 ভ্যালেন্স ইলেক্ট্রন
- গ্রুপ 13: 3 ভ্যালেন্স ইলেক্ট্রন
- গ্রুপ 14: 4 ভ্যালেন্স ইলেক্ট্রন
- গ্রুপ 15: 5 ভ্যালেন্স ইলেক্ট্রন
- গ্রুপ 16: 6 ভ্যালেন্স ইলেক্ট্রন
- গ্রুপ 17: 7 ভ্যালেন্স ইলেক্ট্রন
- গ্রুপ 18: 8 ভ্যালেন্স ইলেকট্রন (হিলিয়াম বাদে, যার 2 রয়েছে)
- আমাদের উদাহরণে, যেহেতু কার্বন 14 টি গ্রুপে রয়েছে তাই আমরা বলতে পারি যে কার্বনের একটি পরমাণু রয়েছে has চার ভ্যালেন্স ইলেকট্রন।
অবস্থান্তর ধাতু
গ্রুপ 3 থেকে 12 এর মধ্যে একটি উপাদান সন্ধান করুন। উপরে উল্লিখিত হিসাবে, 3 থেকে 12 গ্রুপের উপাদানগুলিকে "ট্রানজিশন ধাতু" বলা হয় এবং ভ্যালেন্স ইলেক্ট্রনের ক্ষেত্রে অন্যান্য উপাদানগুলির চেয়ে আলাদা আচরণ করে। এই বিভাগে, আমরা ব্যাখ্যা করব কীভাবে, একটি নির্দিষ্ট পরিমাণে, প্রায়শই এই পরমাণুগুলিতে ভ্যালেন্স ইলেকট্রনগুলি অর্পণ করা সম্ভব হয় না।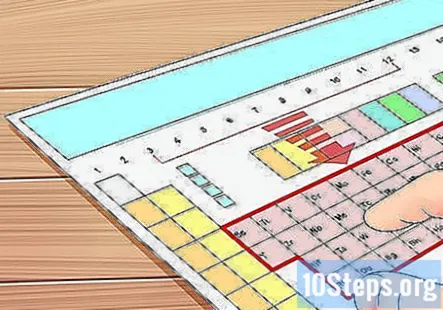
- উদাহরণস্বরূপ, আসুন আমরা ট্যান্টালাম (টা), উপাদানটি বেছে নিন the পরবর্তী কয়েকটি পদক্ষেপে আমরা এর ভ্যালেন্স ইলেক্ট্রনগুলি খুঁজে পাই (বা, কমপক্ষে, চেষ্টা করুন প্রতি.)
- দ্রষ্টব্য যে রূপান্তর ধাতুগুলির মধ্যে ল্যান্থানাইড এবং অ্যাক্টিনাইড সিরিজ অন্তর্ভুক্ত থাকে (এটি "বিরল পৃথিবী ধাতু" নামেও পরিচিত) - দুটি সারি উপাদানগুলির মধ্যে যা সাধারণত টেবিলে বাকী থাকে যা ল্যান্থানাম এবং অ্যাক্টিনিয়াম দিয়ে শুরু হয়। এই উপাদানগুলি সমস্ত সম্পর্কিত গ্রুপ 3 পর্যায় সারণির।
বুঝুন যে রূপান্তর ধাতুগুলিতে "traditionalতিহ্যবাহী" ভ্যালেন্স ইলেকট্রন নেই। অন্যান্য পর্যায় সারণির মতো কেন রূপান্তর ধাতু সত্যই "কাজ" করে না তা বোঝার জন্য ইলেক্ট্রনগুলি পরমাণুর সাথে যেভাবে আচরণ করে সে সম্পর্কে একটু ব্যাখ্যা প্রয়োজন। দ্রুত চালানোর জন্য নীচে দেখুন বা উত্তরের ডানদিকে পেতে এই পদক্ষেপটি এড়িয়ে যান।
- ইলেক্ট্রন যেমন একটি পরমাণুর সাথে যুক্ত হয়, সেগুলি বিভিন্ন "কক্ষপথে" রূপান্তরিত হয় - মূলত ইলেক্ট্রনগুলি যে নিউক্লিয়াসের মধ্যে জমায়েত হয় তার চারপাশের বিভিন্ন অঞ্চলে। সাধারণত, ভ্যালেন্স ইলেকট্রনগুলি বহিস্থতম শেলের ইলেক্ট্রন হয় - অন্য কথায় সর্বশেষ ইলেক্ট্রন যুক্ত হয় ।
- ইলেকট্রনগুলি বহির্মুখীতে যুক্ত করা হলে এখানে ব্যাখ্যা করার জন্য কিছুটা জটিল জটিল কারণগুলি d একটি রূপান্তর ধাতুর শেল (আরও নীচে এটি), শেলটিতে প্রবেশকারী প্রথম ইলেক্ট্রনগুলি স্বাভাবিক ভ্যালেন্স ইলেক্ট্রনগুলির মতো কাজ করতে থাকে তবে তার পরে, তারা না করে এবং অন্যান্য কক্ষপথীয় স্তর থেকে ইলেক্ট্রনগুলি কখনও কখনও পরিবর্তে ভ্যালেন্স ইলেক্ট্রন হিসাবে কাজ করে। এর অর্থ এটি যে কীভাবে ব্যবহৃত হয় তার উপর নির্ভর করে কোনও পরমাণুর একাধিক সংখ্যক ভ্যালেন্স ইলেক্ট্রন থাকতে পারে।
গ্রুপ নম্বরের ভিত্তিতে ভ্যালেন্স ইলেকট্রনের সংখ্যা নির্ধারণ করুন। আবার, আপনি যে উপাদানটির পরীক্ষা করছেন তার গ্রুপ নম্বর আপনাকে এর ভ্যালেন্স ইলেকট্রন বলতে পারে। তবে, রূপান্তর ধাতুগুলির জন্য, এমন কোনও প্যাটার্ন নেই যা আপনি অনুসরণ করতে পারেন - গ্রুপ নম্বরটি বেশিরভাগ সম্ভাব্য সংখ্যক ভ্যালেন্স ইলেক্ট্রনের সাথে সামঞ্জস্য হয়। এইগুলো: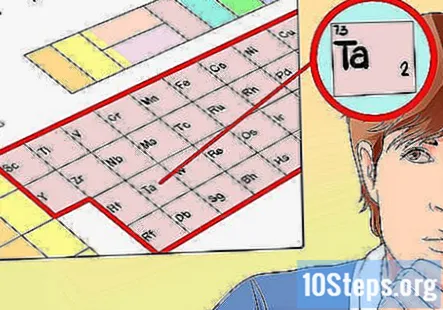
- গ্রুপ 3: 3 ভ্যালেন্স ইলেক্ট্রন
- গ্রুপ 4: 2 থেকে 4 ভ্যালেন্স ইলেক্ট্রন
- গ্রুপ 5: 2 থেকে 5 ভ্যালেন্স ইলেক্ট্রন
- গ্রুপ 6: 2 থেকে 6 ভ্যালেন্স ইলেক্ট্রন
- গ্রুপ 7: 2 থেকে 7 ভ্যালেন্স ইলেক্ট্রন
- গ্রুপ 8: 2 বা 3 ভ্যালেন্স ইলেক্ট্রন
- গ্রুপ 9: 2 বা 3 ভ্যালেন্স ইলেক্ট্রন
- গ্রুপ 10: 2 বা 3 ভ্যালেন্স ইলেকট্রন
- গ্রুপ 11: 1 বা 2 ভ্যালেন্স ইলেকট্রন
- গ্রুপ 12: 2 ভ্যালেন্স ইলেক্ট্রন
- আমাদের উদাহরণস্বরূপ, যেহেতু ট্যানটালাম 5 গ্রুপে রয়েছে তাই আমরা বলতে পারি যে এটির মধ্যে রয়েছে দুই এবং পাঁচটি ভ্যালেন্স ইলেকট্রনপরিস্থিতি উপর নির্ভর করে।
পার্ট 2 এর 2: একটি বৈদ্যুতিন কনফিগারেশন সহ ভ্যালেন্স ইলেকট্রন সন্ধান করা
কীভাবে ইলেক্ট্রন কনফিগারেশন পড়তে হয় তা শিখুন। কোনও উপাদানটির ভ্যালেন্স ইলেক্ট্রনগুলি সন্ধানের আর একটি উপায় হ'ল ইলেক্ট্রন কনফিগারেশন নামে পরিচিত। এগুলি প্রথমে জটিল দেখায় তবে এগুলি অক্ষর এবং সংখ্যা সহ একটি পরমাণুতে বৈদ্যুতিন কক্ষপথ উপস্থাপনের একমাত্র উপায় এবং আপনি কী দেখছেন তা জানার পরে এগুলি সহজ।
- আসুন সোডিয়াম (না) উপাদানটির জন্য একটি উদাহরণের কনফিগারেশনটি দেখি:
- 1s2s2p3s
- লক্ষ্য করুন যে এই বৈদ্যুতিন কনফিগারেশনটি কেবল একটি পুনরাবৃত্তি স্ট্রিং যা এর আগে চলে যায়:
- (সংখ্যা) (চিঠি) (সংখ্যা) (চিঠি) ...
- ... ইত্যাদি। দ্য (সংখ্যা) (চিঠি) অংশটি ইলেক্ট্রন অরবিটালের নাম এবং সেই কক্ষপথে ইলেকট্রনের সংখ্যা - এটিই!
- সুতরাং, আমাদের উদাহরণস্বরূপ, আমরা বলব যে সোডিয়াম আছে 1s কক্ষপথে 2 ইলেকট্রন প্লাস 2s কক্ষপথে 2 ইলেকট্রন প্লাস 2 পি অরবিটালে 6 ইলেকট্রন প্লাস 3s কক্ষপথে 1 ইলেকট্রন এটি মোট ১১ টি ইলেক্ট্রন - সোডিয়াম হ'ল উপাদান সংখ্যা ১১, সুতরাং এটি বোঝা যায়।
- মনে রাখবেন যে প্রতিটি সাব-শেলের একটি নির্দিষ্ট বৈদ্যুতিন ক্ষমতা রয়েছে। তাদের বৈদ্যুতিন ক্ষমতা নিম্নরূপ:
- s: 2 বৈদ্যুতিন ক্ষমতা
- পি: 6 বৈদ্যুতিন ক্ষমতা
- d: 10 বৈদ্যুতিন ক্ষমতা
- f: 14 বৈদ্যুতিন ক্ষমতা
- আসুন সোডিয়াম (না) উপাদানটির জন্য একটি উদাহরণের কনফিগারেশনটি দেখি:
আপনি যে উপাদানটি পরীক্ষা করছেন তার জন্য বৈদ্যুতিন কনফিগারেশনটি সন্ধান করুন। একবার আপনি কোনও উপাদানের বৈদ্যুতিন কনফিগারেশনটি জানতে পারলে, এর ভ্যালেন্স ইলেক্ট্রনগুলির সংখ্যা সন্ধান করা বেশ সহজ (তবে অবশ্যই ট্রানজিশন ধাতুগুলির জন্য)) যদি আপনাকে গেট-গো থেকে কনফিগারেশন দেওয়া হয় তবে আপনি পরবর্তী পদক্ষেপে যেতে পারেন। আপনি যদি এটি নিজের সন্ধান করতে চান তবে নীচে দেখুন:
- ওগেনেসন (ওজি), উপাদান ১১৮ এর জন্য সম্পূর্ণ ইলেক্ট্রন কনফিগারেশন পরীক্ষা করুন, যা পর্যায় সারণির শেষ উপাদান। এটি কোনও উপাদানের সর্বাধিক ইলেক্ট্রন রয়েছে, সুতরাং এর বৈদ্যুতিন কনফিগারেশনটি অন্যান্য উপাদানগুলির মধ্যে আপনি যে সমস্ত সম্ভাবনার মুখোমুখি হতে পারেন তা প্রদর্শন করে:
- 1s2s2p3s3p4s3d4p5s4d5p6s4f5d6p7s5f6d7p
- এখন আপনার কাছে এটি রয়েছে, অন্য পরমাণুর বৈদ্যুতিন কনফিগারেশনটি সন্ধান করার জন্য আপনাকে যা করতে হবে কেবল তা শুরু থেকে ইলেক্ট্রন শেষ হয়ে না যাওয়া পর্যন্ত এই প্যাটার্নটি পূরণ করা। এটি শোনার চেয়ে সহজ। উদাহরণস্বরূপ, আমরা যদি ক্লোরিন (সিএল) এর কক্ষপথের চিত্রটি তৈরি করতে চাই, উপাদান 17, যার 17 টি ইলেক্ট্রন রয়েছে, আমরা এটি এটি করব:
- 1s2s2p3s3p
- লক্ষ্য করুন যে ইলেক্ট্রনগুলির সংখ্যা 17: 2 + 2 + 6 + 2 + 5 = 17 পর্যন্ত যুক্ত হয়েছে You আপনাকে কেবল চূড়ান্ত কক্ষপথের সংখ্যাটি পরিবর্তন করতে হবে - বাকীটি একইরূপে চূড়ান্তটি সম্পূর্ণ পূর্ণ হওয়ার আগে অরবিটালগুলি রয়েছে ।
- ইলেক্ট্রন কনফিগারেশন সম্পর্কে আরও জানতে এই নিবন্ধটি দেখুন।
- ওগেনেসন (ওজি), উপাদান ১১৮ এর জন্য সম্পূর্ণ ইলেক্ট্রন কনফিগারেশন পরীক্ষা করুন, যা পর্যায় সারণির শেষ উপাদান। এটি কোনও উপাদানের সর্বাধিক ইলেক্ট্রন রয়েছে, সুতরাং এর বৈদ্যুতিন কনফিগারেশনটি অন্যান্য উপাদানগুলির মধ্যে আপনি যে সমস্ত সম্ভাবনার মুখোমুখি হতে পারেন তা প্রদর্শন করে:
অক্টেট বিধি দিয়ে কক্ষপথের কক্ষগুলিতে ইলেক্ট্রনগুলি অর্পণ করুন। ইলেক্ট্রন যেমন পরমাণুর সাথে যুক্ত হয়, উপরোক্ত আদেশ অনুসারে এগুলি বিভিন্ন কক্ষপথে পড়ে - প্রথম দুটি 1s কক্ষপথে যায়, তার পরের দুটি 2s কক্ষপথে যায়, তার পরের ছয়টি 2p কক্ষপথে যায় এবং শীঘ্রই. যখন আমরা রূপান্তর ধাতুর বাইরে পরমাণু নিয়ে কাজ করি, আমরা বলি যে এই কক্ষপথগুলি নিউক্লিয়াসের চারপাশে "কক্ষপথের শাঁস" গঠন করে, প্রতিটি ক্রমাগত শেলটি আগের চেয়ে আরও বাইরে থাকে। প্রথম শেলটি ছাড়াও, যা কেবল দুটি ইলেক্ট্রন ধরে রাখতে পারে, প্রতিটি শেলের আটটি ইলেক্ট্রন থাকতে পারে (ট্রানজিশন ধাতুগুলির সাথে কাজ করার সময় আবার বাদে।) এটিকে বলা হয় ওকেট বিধি।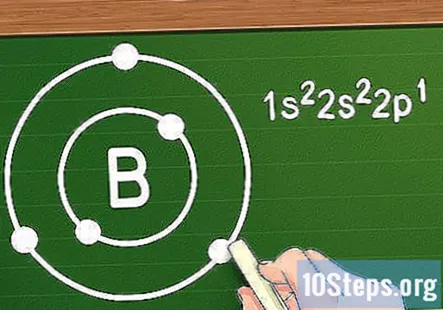
- উদাহরণস্বরূপ, ধরা যাক আমরা বোর্ন (বি) উপাদানটির দিকে তাকিয়ে আছি। যেহেতু এর পারমাণবিক সংখ্যা পাঁচটি, আমরা জানি যে এর পাঁচটি ইলেক্ট্রন রয়েছে এবং এর বৈদ্যুতিন কনফিগারেশনটি দেখতে এইরকম: 1s2s2p। যেহেতু প্রথম কক্ষপথের শেলটিতে মাত্র দুটি ইলেক্ট্রন রয়েছে, আমরা জানি যে বোরনের দুটি শাঁস রয়েছে: একটিতে 2 1s ইলেক্ট্রন রয়েছে এবং একটি 2s এবং 2 পি অরবিটাল থেকে তিনটি ইলেকট্রন সহ রয়েছে।
- অন্য উদাহরণ হিসাবে, ক্লোরিনের মতো একটি উপাদান (1s2s2p3s3p) এর মধ্যে তিনটি কক্ষীয় শেল থাকবে: একটিতে দুটি 1s ইলেক্ট্রনযুক্ত একটি, দুটি 2s ইলেক্ট্রন এবং ছয় 2p ইলেক্ট্রন সহ একটি এবং দুটি 3s ইলেক্ট্রন এবং পাঁচ 3p ইলেক্ট্রনযুক্ত একটি থাকবে।
বাইরেরতম শেলের মধ্যে ইলেকট্রনের সংখ্যা সন্ধান করুন। এখন আপনি নিজের উপাদানটির বৈদ্যুতিন শেলগুলি জানেন, ভ্যালেন্স ইলেক্ট্রনগুলি সন্ধান করা সহজ: কেবলমাত্র বহিরাগত শেলের মধ্যে ইলেকট্রনের সংখ্যা ব্যবহার করুন। যদি বাইরের শেলটি পূর্ণ থাকে (অন্য কথায়, যদি এটিতে আটটি ইলেক্ট্রন থাকে বা, প্রথম শেলের জন্য, দুটি), উপাদানটি জড় হয় এবং অন্যান্য উপাদানগুলির সাথে সহজেই প্রতিক্রিয়া দেখায় না। আবার, তবে, জিনিসগুলি রূপান্তর ধাতুগুলির জন্য এই নিয়মগুলি পুরোপুরি অনুসরণ করে না।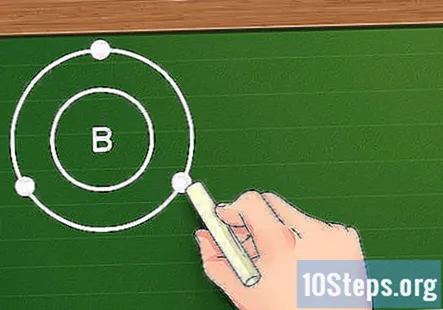
- উদাহরণস্বরূপ, যদি আমরা বোরনের সাথে কাজ করি, যেহেতু দ্বিতীয় শেলের মধ্যে তিনটি ইলেক্ট্রন রয়েছে, আমরা বলতে পারি যে বোরন রয়েছে তিন যথোপযুক্ত সৃষ্টিকর্তা.
কক্ষপথের সারিগুলি অরবিটাল শেল শর্টকাট হিসাবে ব্যবহার করুন। পর্যায় সারণির অনুভূমিক সারিগুলিকে উপাদান বলা হয় "পিরিয়ডস" টেবিলের শীর্ষ থেকে শুরু করে, প্রতিটি সময়কালের সংখ্যার সাথে মিলে যায় বৈদ্যুতিন শেল পিরিয়ডের পরমাণুগুলির অধিকার রয়েছে। কোনও উপাদানকে কত ভ্যালেন্স ইলেকট্রন রয়েছে তা নির্ধারণ করতে আপনি এটি শর্টকাট হিসাবে ব্যবহার করতে পারেন - ইলেক্ট্রনগুলি গণনা করার সময় তার পিরিয়ডের বাম দিক থেকে শুরু করুন। আবারও, আপনি এই পদ্ধতির সাহায্যে রূপান্তর ধাতুগুলি উপেক্ষা করতে চাইবেন, যার মধ্যে গ্রুপগুলি 3-12 রয়েছে।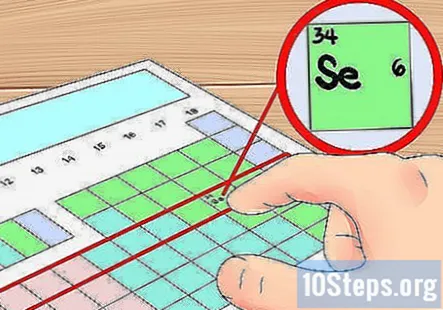
- উদাহরণস্বরূপ, আমরা জানি সেলেনিয়াম উপাদানটির চারটি কক্ষপথ রয়েছে, কারণ এটি চতুর্থ সময়কালে রয়েছে। যেহেতু এটি চতুর্থ সময়কালে (রূপান্তর ধাতু উপেক্ষা করে) বাম দিক থেকে ষষ্ঠ উপাদান, তাই আমরা জানি যে বাইরের চতুর্থ শেলের ছয়টি ইলেক্ট্রন রয়েছে এবং এইভাবে সেলেনিয়াম রয়েছে ছয় ভ্যালেন্স ইলেক্ট্রন।
সম্প্রদায় প্রশ্ন এবং উত্তর
আমরা কীভাবে ভ্যালেন্স ইলেকট্রন গণনা করব?
উপাদানগুলির বৈদ্যুতিন কনফিগারেশনগুলি নির্ধারণ করে ভ্যালেন্স ইলেক্ট্রনগুলি পাওয়া যায়। তারপরে বাইরেরতম শেলের মধ্যে ইলেক্ট্রনগুলির সংখ্যা সেই উপাদানটিতে মোট ভ্যালেন্স ইলেকট্রন দেয়।
যদি কোনও পরমাণুতে 33 টি ইলেকট্রন থাকে তবে কতটি ভ্যালেন্স ইলেকট্রন রয়েছে?
যদি পরমাণু আয়ন না হয়, তবে আমরা বলতে পারি যে পরমাণুর 33 টি প্রোটন রয়েছে। এর অর্থ এটি 33 উপাদান, যা আর্সেনিক। তারপরে আমরা জানি যে এটি কোনও রূপান্তর ধাতু নয়, তাই আমরা এর গ্রুপ নম্বরের একক সংখ্যা 5 দেখতে পেয়েছি এবং এর অর্থ এটিতে 5 ভ্যালেন্স ইলেকট্রন রয়েছে r
আমি হিলিয়ামের পারমাণবিক সংখ্যা কীভাবে নির্ধারণ করব?
প্রোটনের সংখ্যা পারমাণবিক সংখ্যার সমান।
কেন ইলেকট্রনগুলি নেতিবাচক চার্জ অর্জন করে এবং ইতিবাচক চার্জ নয়?
পরমাণুগুলি ইলেকট্রন লাভ করে বা হারাতে পারে, নেতিবাচক চার্জ দেয় কারণ প্রোটনের ইতিবাচক চার্জ থাকে এবং তারা শক্তিশালী পারমাণবিক শক্তি দ্বারা নিউক্লিয়াসে ধারণ করে। এটি মহাবিশ্বের চারটি স্বতন্ত্র শক্তির মধ্যে একটি: মাধ্যাকর্ষণ, তড়িচ্চুম্বকত্ব, দুর্বল শক্তি এবং শক্তিশালী পারমাণবিক শক্তি। এটি শক্তিশালী হয়ে উঠতে পারে কারণ প্রোটনগুলি একে অপরকে বিতাড়িত করে তবে তারা নিউক্লিয়াসে সত্যই একত্রে থাকে (শক্তিশালী শক্তি দ্বারা ধারণকৃত নিউট্রনগুলির সাথেও।) ধারণাটি এই যে শক্তিশালী শক্তি অত্যন্ত শক্তিশালী তবে কেবল খুব ছোট দূরত্বে over ক্ষুদ্র অতি শক্তিশালী হুক চিন্তা করুন। প্রোটন এবং নিউট্রন হুক করার জন্য আপনার কাছে একটি নক্ষত্র, একটি সুপারনোভা বা পারমাণবিক বিস্ফোরণের মত বিশাল শক্তির প্রয়োজন।
মহৎ গ্যাসের ভারসাম্য ইলেক্ট্রন কী?
নোবেল গ্যাসগুলিতে আটটি ভ্যালেন্স ইলেক্ট্রন রয়েছে - কোনও উপাদানের জন্য সবচেয়ে স্থিতিশীল রাষ্ট্র।
নাইট্রোজেনের কেন 6 টি ভারসাম্য ইলেক্ট্রন রয়েছে তবে এটি 15 গ্রুপে রয়েছে?
নাইট্রোজেনের কেবল পাঁচটি ভারসাম্য ইলেক্ট্রন রয়েছে কারণ এটি গ্রুপ 5 এ রয়েছে, যদিও এটি প্রকৃতপক্ষে 15 দলের মধ্যে রয়েছে আপনি ট্রানজিশনাল ধাতুগুলি উপেক্ষা করতে চলেছেন কারণ এই গ্রুপগুলির ভ্যালেন্স ইলেক্ট্রন নির্ধারণের বিভিন্ন উপায় রয়েছে। সুতরাং: গ্রুপ 13 এর অর্থ গ্রুপ 3 তত এবং আরও
একটি পরমাণুতে 7 প্রোটন, 8 টি নিউরন এবং 7 টি ইলেক্ট্রন থাকে। এর ভ্যালেন্স শেলটিতে ইলেকট্রনের সংখ্যা কত?
যে উপাদানটিতে 7 প্রোটন রয়েছে তা হ'ল নাইট্রোজেন। নাইট্রোজেন উপাদানগুলির কলামে ভ্যালেন্স শেলটিতে 5 টি ইলেক্ট্রন রয়েছে। নির্দিষ্ট উপাদানটিতে ভ্যালেন্স ইলেক্ট্রনের সংখ্যা খুঁজে পাওয়ার জন্য নিউট্রনের সংখ্যা অপ্রাসঙ্গিক।
পর্যায় সারণিতে সাতটি বহিরাগত শেল ইলেকট্রনযুক্ত পরমাণুগুলি কোথায় অবস্থিত?
জড় গ্যাসগুলির পাশে ডান হাতের দ্বিতীয় থেকে শেষ কলামটি দেখুন।
ভ্যালেন্স ইলেক্ট্রন কী?
ভ্যালেন্স ইলেক্ট্রন হ'ল একটি ইলেক্ট্রন যা পরমাণুর বাইরের অংশে পাওয়া যায় এবং ভাগ বা ভাগ করে নেওয়া যায় taken
পর্যায় সারণিতে থাকা উপাদানগুলিতে কেন ভ্যালেন্স ইলেক্ট্রনগুলির বিভিন্ন সংখ্যা থাকে?
তাদের বিভিন্ন রাসায়নিক কাঠামো রয়েছে। ভ্যালেন্স ইলেক্ট্রনগুলিই রাসায়নিক বিক্রিয়া তৈরি করে।
পরামর্শ
- দ্রষ্টব্য যে বৈদ্যুতিন কনফিগারেশনগুলি কনফিগারেশনের শুরুতে কক্ষপথে দাঁড়াতে নোবেল গ্যাসগুলি (গ্রুপ 18 এর উপাদানগুলি) ব্যবহার করে এক ধরণের শর্টহ্যান্ডে লেখা যেতে পারে। উদাহরণস্বরূপ, সোডিয়ামের ইলেক্ট্রন কনফিগারেশনটি 3s1 লেখা যেতে পারে - মূলত এটি নিওনের মতোই, তবে 3s কক্ষপথে আরও একটি ইলেকট্রন সহ।
- ট্রানজিশন ধাতুতে ভ্যালেন্স সাবশেল থাকতে পারে যা সম্পূর্ণরূপে ভরা হয় না। রূপান্তর ধাতুগুলিতে ভ্যালেন্স ইলেকট্রনের সঠিক সংখ্যা নির্ধারণে কোয়ান্টাম তত্ত্বের নীতিগুলি জড়িত যা এই নিবন্ধের আওতার বাইরে beyond
- লক্ষ্য রাখবেন যে পর্যায় সারণী দেশ থেকে দেশে আলাদা হয়। সুতরাং, দয়া করে পরীক্ষা করুন যে আপনি বিভ্রান্তি এড়াতে সঠিক, আপডেট হওয়া ব্যবহার করছেন।
- ভ্যালেন্স ইলেকট্রন সন্ধানের জন্য কখন শেষ কক্ষপথ থেকে যুক্ত বা বিয়োগ করবেন তা নিশ্চিত হন।
আপনার যা প্রয়োজন
- উপাদানগুলির পর্যায় সারণি
- পেন্সিল
- কাগজ
উইকিউইউতে প্রতিদিন, আমরা আপনাকে এমন নির্দেশাবলী এবং তথ্যে অ্যাক্সেস দেওয়ার জন্য কঠোর পরিশ্রম করি যা আপনাকে আরও সুরক্ষিত, স্বাস্থ্যকর, বা আপনার মঙ্গল বাড়িয়ে তুলতে আপনাকে আরও উন্নত জীবনযাপন করতে সহায়তা করবে। বর্তমান জনস্বাস্থ্য এবং অর্থনৈতিক সংকটগুলির মধ্যে, যখন বিশ্ব নাটকীয়ভাবে পরিবর্তন হচ্ছে এবং আমরা সকলেই প্রতিদিনের জীবনে পরিবর্তনগুলি শিখছি এবং খাপ খাইয়ে নিচ্ছি, মানুষের আগের চেয়ে আরও বেশি উইকি দরকার। আপনার সমর্থন উইকিউকে আরও গভীরতর চিত্রিত নিবন্ধ এবং ভিডিওগুলি তৈরি করতে এবং বিশ্বস্ত লক্ষ লক্ষ মানুষের সাথে আমাদের বিশ্বস্ত ব্র্যান্ডের নির্দেশিক সামগ্রী ভাগ করতে সহায়তা করে। আজকে উইকিতে কীভাবে অবদান রাখবেন তা বিবেচনা করুন।